近日,美國食品藥品監督管理局(Food and Drug Administration;簡稱FDA)官網公布:貝達藥業恩沙替尼臨床研究中心符合美國FDA制定的GCP(藥物臨床試驗質量管理規范),順利通過FDA核查,這是繼8月公司及控股子公司Xcovery通過美國FDA的臨床BIMO(Bioresearch Monitoring,生物研究監測)相關PAI(Pre-Approval Inspection,批準前檢查)現場核查、原料藥CMC(Chemical Manufacture and Control,化學、生產與控制)PAI現場核查后,臨床核查也順利通過,標志著恩沙替尼的臨床研究符合國際標準,距在美獲批上市再近一步。
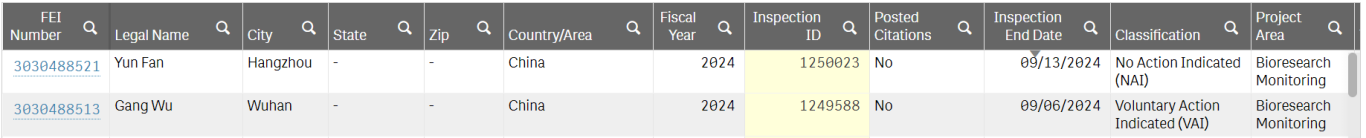
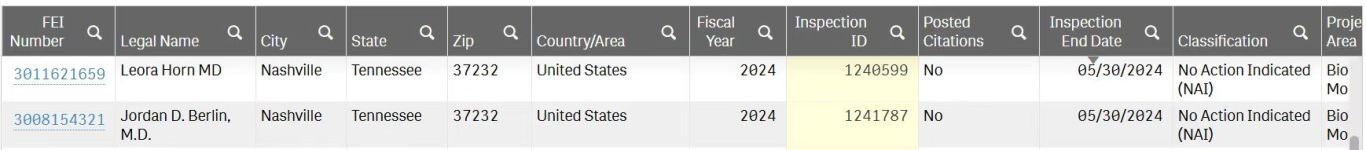
△來源:FDA官網
臨床研究是藥物研發過程中的一個重要環節,美國FDA針對臨床試驗研究制定了嚴格的管理規范,包括臨床研究方案執行、數據準確性與完整性、數據的使用都要符合GCP和規范的SOP運行,旨在確保藥物的安全性、有效性得到正確評估并且確保受試者的權利和安全得到保護。
FDA檢查員于2024年9月2日至9月13 日對恩沙替尼中國的兩個臨床研究中心進行了現場檢查。FDA檢查員逐項審閱了監管文件、申辦方通信、研究者資質文件、原始病歷、實驗室報告、病例報告表、試驗藥品的發放回收記錄、儲存條件的文件,走訪了GCP藥房,與PI和研究團隊訪談了研究者職責和方案的特定流程。經過10天全面系統的核查,FDA檢查員充分肯定臨床研究的文件記錄的完整性和數據的科學性,認為臨床研究中心流程清晰,質量管理嚴格,試驗數據客觀真實可靠,實施符合方案要求,主要研究者和研究團隊各成員盡職盡責,嚴謹的工作方式保證臨床試驗質量,符合美國FDA制定的GCP管理規范,并且對疫情期間研究機構制定的相應管理措施保障了受試者的治療和數據的完整性和科學性給與中肯的認可。
貝達藥業副總裁張惠軍表示,這是公司首次迎接美國FDA臨床現場核查,也是FDA審評審批的關鍵環節,國內的兩個研究中心順利通過FDA現場核查,離不開研究中心及貝達研究團隊每一位同事的辛勤工作,反映了他們一貫嚴謹科學的工作作風,也離不開公司的全方位支持。FDA臨床現場核查通過標志著恩沙替尼關鍵審評審批里程碑的達成,期待恩沙替尼早日在美國獲批上市。
Xcovery 首席執行官桑凌表示,很高興恩沙替尼美國的臨床研究中心順利通過核查,作為貝達的首個海外NDA項目,我們將積極推進后續的工作,爭取早日取得最后的通行證,造福更多患者。
貝達藥業董事長丁列明博士表示,恩沙替尼境內外臨床中心都順利通過FDA現場核查,是貝達藥業和臨床研究中心一直嚴格貫徹執行GCP標準的結果,讓我們對恩沙替尼在美獲批充滿信心,也為貝達繼續開拓國際市場奠定了堅實基礎。未來,公司仍將堅持高標準、嚴要求,為患者持續提供高品質的新藥。
下一條: 貝達藥業注射用MCLA-129 晚期實體瘤臨床試驗獲批開展
